에이치엘비, 리보세라닙 선양낭성암 FDA 희귀의약품 지정
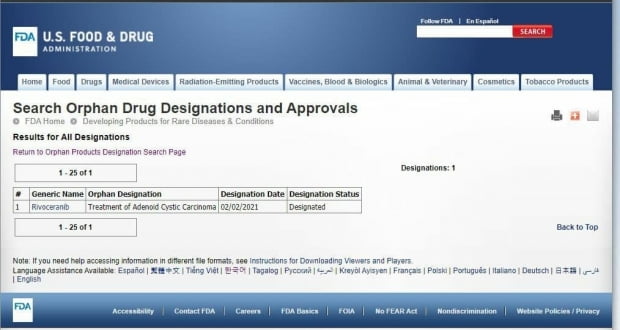
선양낭성암은 침샘암으로도 불린다. 미국과 유럽에 환자가 많은 희귀암종이다. 현재 승인받은 표준치료제가 없다. 에이치엘비의 미국 자회사인 엘레바는 선양낭성암 치료제 개발을 위해 미국과 한국에서 총 72명의 환자를 대상으로 임상 2상을 진행하고 있다.
FDA의 희귀의약품 지정은 희귀·난치성 질병의 치료제 개발 및 허가가 원활하게 이뤄질 수 있도록 지원하는 제도다.
희귀의약품으로 지정되면 신속심사(패스트트랙)가 적용돼 임상시험 승인 및 허가 기간이 단축된다. 전문의약품 허가 신청비용이 면제되고 세금감면 혜택도 받는다. 허가를 취득한 후에는 7년간 시장 독점권이 부여된다.
에이치엘비는 2017년 FDA로부터 리보세라닙의 위암에 대한 희귀의약품 지정을 받았다. 현재 위암 3,4차 치료제로 판매허가신청(NDA)을 준비 중이다.
리보세라닙의 간암 1차 치료제 임상 3상, 대장암 3차 치료제 임상 2상, 위암 2차 치료제 임상 2상도 각각 미국에서 진행하고 있다.
박인혁 기자 hyuk@hankyung.com
-
기사 스크랩
-
공유
-
프린트





![벅셔 주총장 팀쿡 등장…버핏은 애플 지분 13% 팔았다 [오마하 현장 리포트]](https://timg.hankyung.com/t/560x0/photo/202405/B20240505014502147.jpg)