[바이오번역 한경바이오인투] 국내 1호 셀트리온 코로나 치료제…식약처, 고위험군 환자에 사용 허가
페이지 정보
작성자바이오인투 작성일 21-02-08 04:30본문
<한경바이오인투는 (주)한국경제신문이 운영하는 제약, 임상, 의학, 약학 분야에 특화된 바이오산업 전문 번역업체입니다.>
셀트리온의 코로나19 항체치료제 ‘렉키로나(성분명 레그단비맙·CT-P59)’가 세계에서 세 번째로 판매 허가를 받았다. 처방 대상은 고령자와 기저질환자 등 고위험군 성인 환자다.
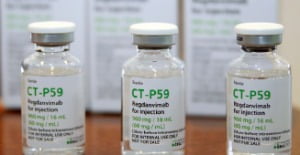
식품의약품안전처는 5일 최종점검위원회를 열어 셀트리온의 렉키로나에 조건부 품목 허가 결정을 내렸다. 식약처는 회의 후 “렉키로나 960㎎에 대해 임상 3상 시험 결과 제출을 조건으로 품목 허가를 결정했다”고 설명했다.
이날 허가로 렉키로나는 세계에서 세 번째로 규제당국의 허가를 받은 코로나19 항체치료제가 됐다. 앞서 미국 식품의약국(FDA)은 일라이 릴리와 리제네론의 코로나19 치료제를 조건부 허가했다. 셀트리온은 유럽과 미국에서도 허가를 받을 예정이다.
식약처는 렉키로나 조건부 허가를 위해 3단계 검증을 거쳤다. 법정 자문기구인 중앙약사심의위원회를 시작으로 코로나19 치료제·백신 안전성·효과성 검증 자문단, 최종점검위원회 등이 모두 조건부 허가를 요청했다. 이날 진행된 최종점검위는 오일환 중앙약심위 생물의약품분과위원장과 외부 전문가 3인, 식약처장 등 5명이 참석했다.
이들은 “임상시험을 비롯해 비임상시험, 품질, 위해성, 관리계획, 제조·품질관리 등 허가 심사에 필요한 주요 자료가 충실히 제출됐다”며 “안전성·효과성과 관련한 분야별 심층 자료와 현지조사 결과 등을 검토한 결과 품목허가에 문제가 없는 것으로 판단했다”고 설명했다.
셀트리온은 렉키로나를 맞으면 경증 환자가 중증으로 악화될 확률이 54% 줄어들고, 폐렴 증상을 보이는 환자의 치료 기간도 5~6일 단축된다는 내용의 임상 2상 결과를 발표했다. 한국과 루마니아, 미국, 스페인 등 코로나19 환자 327명을 대상으로 했다. 현재 10여 개국에서 1172명의 경증·중등증 환자를 대상으로 임상 3상을 진행하고 있다. 셀트리온은 정부와 치료제의 첫 번째 투약 시기를 조율하고 있다.
김우섭 기자 duter@hankyung.com
ⓒ 한경닷컴, 무단전재 및 재배포 금지
관련링크
댓글목록
등록된 댓글이 없습니다.

