[바이오번역 한경바이오인투] “압타머사이언스, 내년까지 매출 확대 및 기술이전 기대”
페이지 정보
작성자바이오인투 작성일 21-10-22 09:25본문
<한경바이오인투는 (주)한국경제신문이 운영하는 제약, 임상, 의학, 약학 분야에 특화된 바이오산업 전문 번역업체입니다.>
김상표 연구원은 “압타머 발굴 원천기술 특허 만료 후 압타머 치료제에 대한 글로벌 대형제약사(빅파마)의 관심이 커지고 있다”며 “기존 항체 기반 의약품 시장의 미충족 수요에 기반한 압타머 제품 개발이 이뤄지면서 글로벌 압타머 시장규모는 2025년 59억달러(약 6조9000억원)에 이를 것”이라 전망했다.
압타머 기반 신제품 치료제 및 진단분야의 성장 동력(모멘텀)이 더욱 강화될 것이란 예상이다.
김 연구원은 “회사는 글로벌 최고 수준의 압타머를 발굴할 수 있는 2세대 ‘셀렉스(SELEX)’ 기술과 기존 압타머 의약품 대비 결합력과 특이성, 안정성이 개선된 2세대 압타머를 가지고 있다”며 “신약 개발에 필요한 응용기술도 있어 경쟁사 대비 빠른 후보물질(파이프라인)별 성과가 기대된다”고 했다.
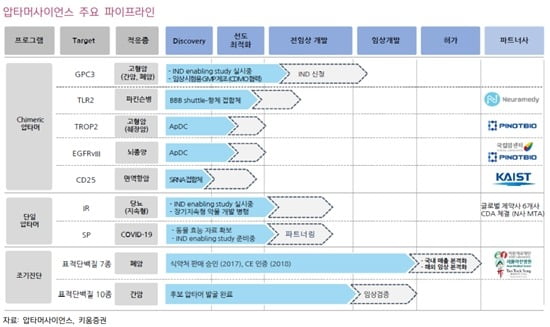
자료 제공=압타머사이언스
파이프라인은 크게 진단과 신약으로 나뉜다. 진단분야에서는 올해 안에 폐암조기진단키트의 보험급여 관련 문제가 해결되면서, 매출이 본격화 될 것으로 봤다. 이 진단키트는 식품의약품안전처 판매 승인과 유럽 제품인증(CE)을 보유하고 있다. 또 현재 중국과 싱가포르에서 임상을 진행하고 있어, 내년 중국 및 동남아 관련 매출 확대도 가시화 될 것이란 전망이다.
신약 부문에서는 ‘간암치료제(AST-201)’와 ‘당뇨치료제(AST-101)’, ‘뇌혈관장벽(BBB) 셔틀 압타머’가 주목할 만한 성과를 낼 것으로 예상했다.
AST-201는 임상시험을 위한 위탁개발생산(CDMO) 선정을 마치고, 공정개발 최적화 단계에 있다. 이를 바탕으로 내년 상반기 임상 1상을 신청할 예정이다.
AST-101는 내년 상반기 임상 1상 진입이 목표다. 김 연구원은 “현재 글로벌 제약사 6개사와 비밀유지조항을 맺은 상태”라며 “1개사와는 후보물질 검증단계(MTA) 계약을 체결해, 당뇨치료 혁신신약으로의 기대감을 높이고 있다”고 했다.
뇌혈관장벽(BBB) 셔틀 플랫폼 기술로는 뉴라메디와 파킨슨병 치료제 공동 연구 및 개발 계약을 체결했다. 김 연구원은 “뇌질환 치료제 개발 경쟁이 가속화되고 ‘트랜스페린 수용체(TfR)’ 매개 셔틀 플랫폼 수요가 늘고 있다”며 “회사의 BBB셔틀 플랫폼은 향후 파킨슨병을 비롯한 뇌질환 치료제 시장에서 선점적인 지위를 지닐 것”이라고 말했다.
이도희 기자
ⓒ 한경닷컴, 무단전재 및 재배포 금지
관련링크
댓글목록
등록된 댓글이 없습니다.

