[바이오번역 한경바이오인투] “네오이뮨텍, 미충족 수요 높은 암종서 병용요법 효과 확인”
페이지 정보
작성자바이오인투 작성일 21-11-16 09:06본문
<한경바이오인투는 (주)한국경제신문이 운영하는 제약, 임상, 의학, 약학 분야에 특화된 바이오산업 전문 번역업체입니다.>
대신증권 분석
대신증권(20,400 0.00%)은 16일 네오이뮨텍(Reg.S)에 대해 미국 면역항암학회(SITC) 발표를 통해 다양한 고형암으로의 임상 확장과 후기 임상의 기반이 될 결과(데이터)를 확인했다고 평가했다. 투자의견과 목표주가는 제시하지 않았다.
네오이뮨텍은 이번 SITC에서 주력 후보물질인 ‘NT-I7’의 대장암(MSS-CRC)과 췌장암에 대한 임상 2a상 중간결과 2건과 신규로 진단된 교모세포종(GBM)에 대한 화학·방사선 치료와의 병용임상 1상 1건 등 총 3건을 포스터로 발표했다.
NT-I7은 ‘헬퍼 T세포(CD4+)’와 ‘킬러 T세포(CD8+)’에 작용하는 면역항암제 후보물질이다. ‘인터루킨-7(IL-7)’ 수용체를 통해 T세포를 활성화시키는 지속형 IL-7 융합 단백질이다.
네오이뮨텍은 이번 SITC에서 주력 후보물질인 ‘NT-I7’의 대장암(MSS-CRC)과 췌장암에 대한 임상 2a상 중간결과 2건과 신규로 진단된 교모세포종(GBM)에 대한 화학·방사선 치료와의 병용임상 1상 1건 등 총 3건을 포스터로 발표했다.
NT-I7은 ‘헬퍼 T세포(CD4+)’와 ‘킬러 T세포(CD8+)’에 작용하는 면역항암제 후보물질이다. ‘인터루킨-7(IL-7)’ 수용체를 통해 T세포를 활성화시키는 지속형 IL-7 융합 단백질이다.
이번 SITC 발표를 통해 교모세포종 췌장암 대장암 등 표준치료법이나 면역관문억제제(CPI)에 대한 반응이 제한적이고 예후가 좋지 않은 환자를 대상으로 새로운 치료법의 가능성을 확인했다는 평가다.
회사는 CPI 투여 이력이 없는 재발성·불응성 대장암 환자 대상 2a상에서 MSD의 면역관문억제제 키트루다와 NT-I7 병용투여의 긍정적인 결과를 확인했다. 임윤진 연구원은 “초록 공개 당시 객관적반응률(ORR) 7%, 질병통제율(DCR) 47%였으나, 포스터 발표 ORR 18%, DCR 59%로 높아진 결과를 확인했다”며 “부분관해(PR) 환자도 1명에서 2명으로 증가했다”고 설명했다.
췌장암에서는 CPI 투여 이력이 없는 환자를 대상으로 키트루다와 병용 투여했을 때 ORR 6%, DCR 29%로 나타났다.
회사는 CPI 투여 이력이 없는 재발성·불응성 대장암 환자 대상 2a상에서 MSD의 면역관문억제제 키트루다와 NT-I7 병용투여의 긍정적인 결과를 확인했다. 임윤진 연구원은 “초록 공개 당시 객관적반응률(ORR) 7%, 질병통제율(DCR) 47%였으나, 포스터 발표 ORR 18%, DCR 59%로 높아진 결과를 확인했다”며 “부분관해(PR) 환자도 1명에서 2명으로 증가했다”고 설명했다.
췌장암에서는 CPI 투여 이력이 없는 환자를 대상으로 키트루다와 병용 투여했을 때 ORR 6%, DCR 29%로 나타났다.
특히 대장암 및 췌장암 환자군에서 림프구 및 ‘줄기세포 유사 기억 T세포(Tscm·Stem-cell memory CD8 T cell)’가 증가함을 확인했다. CPI와 NT-I7 병용 투여 3주차에 CD8+ Tscm은 최대 50배까지 증폭했다. Tscm은 자가 재생 및 분화 능력과 같은 줄기세포의 능력을 보유해, T세포 중 항암 효능이 가장 높다는 설명이다.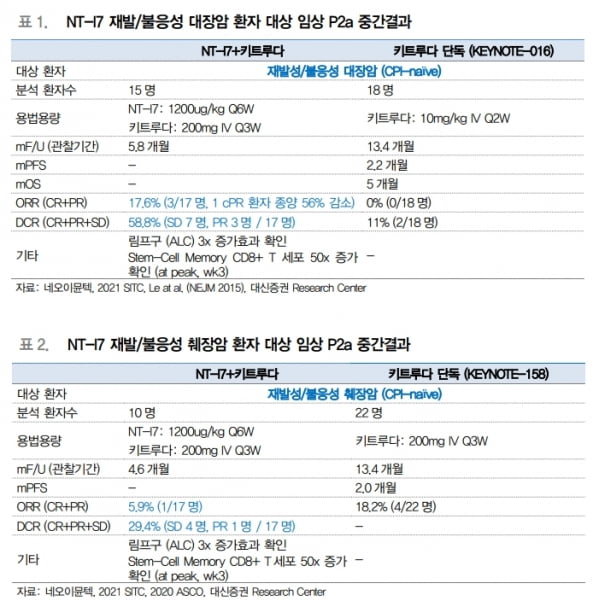
ⓒ 한경닷컴, 무단전재 및 재배포 금지
이와 함께 신규 진단 교모세포종 환자에 NT-I7과 방사선·화학요법 병용 투여한 결과, 림프구 수치가 1000마이크로그램(ug) 이상으로 증가 및 유지됨을 확인했다. 1년 이상 생존율은 표준치료법 25% 대비 94%로 증가했다.
네오이뮨텍은 오는 19일 미국 신경종양학회(SNO)에서 임상 결과를 구두로 발표할 예정이다. 현재 20명 규모에서 50명으로 임상을 확대하고, 내년 상반기 재발 환자를 대상으로 추가 임상을 진행할 계획이다.
임 연구원은 “네오이뮨텍은 CP가I 허가 획득에 실패했거나 반응률이 낮은 암종에 대해 임상 진행 후 폐암 위장관 유방암 등으로 임상을 확대한다는 전략”이라며 “교모세포종은 아이맙이 동일 적응증으로 중국 내 2상을 진행 중인만큼, 중간결과 및 개발현황 공유를 통해 효율적인 임상 개발이 가능할 것”이라고 기대했다.
이어 “고형암 환자 대상의 키트루다 병용 2a상은 비소세포폐암 소세포폐암 삼중음성유방암 난소암 환자군에 대한 임상을 마친 후, 내년 하반기 최종 데이터를 발표할 것”이라고 했다.
김예나 기자
관련링크
댓글목록
등록된 댓글이 없습니다.

