[바이오번역 한경바이오인투] “내년 제약바이오 R&D 성과 기대…삼바·유한양행 최선호”
페이지 정보
작성자바이오인투 작성일 21-11-22 08:38본문
<한경바이오인투는 (주)한국경제신문이 운영하는 제약, 임상, 의학, 약학 분야에 특화된 바이오산업 전문 번역업체입니다.>
박재경 연구원은 22일 “제약·바이오 업종의 원 성장동력인 R&D에 주목하라”고 했다. 국내 제약바이오 기업이 세계 시장에서 꾸준히 주목받고 있으며, 일부 신약은 미국 식품의약국(FDA) 승인을 앞두고 있다는 것이다.
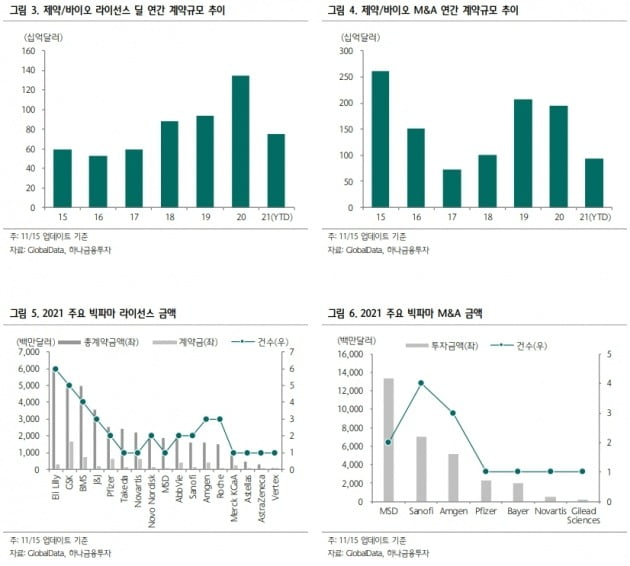
자료 제공=하나금융투자
특히 개념 입증(POC)을 앞둔 플랫폼 기술 기업에 주목하라고 했다. 박 연구원은 “초기 단계의 기술이전은 즉시 수령하는 계약금이 낮고 성과 달성에 오랜 시간이 걸리며 성공 확률도 낮다”며 “임상 결과를 통해 개념을 입증하면 기술의 가치를 크게 높일 수 있다”고 말했다.
지씨셀(102,700 -1.34%)은 제대혈 유래 자연살해(NK) 세포치료제의 최초 임상 결과 발표를 앞두고 있다. 레고켐바이오(48,650 -3.85%)도 자체 항체약물접합체(ADC) 플랫폼의 최초 임상 결과가 내년 상반기에 나올 것으로 봤다.
바이오시밀러(바이오의약품 복제약) 시장에 대한 전망도 내놨다. 블록버스터(연 매출 10억달러 이상 의약품)의 특허 만료가 대거 예정돼있는 점이 성장동력이 될 것이란 분석이다.
향후 10년간 ‘루센티스’ ‘아일리아’ 등 안과 질환 블록버스터와 ‘키트루다’ ‘옵디보’를 필두로 한 면역항암제 블록버스터들의 특허 만료가 기다리고 있다. 특허 만료 의약품의 개수 역시 과거 10년에 비해 2배에 달할 것으로 전망했다.
내년 승인단계에 진입하는 국산 신약에도 관심을 가질 것을 권고했다. 녹십자(230,500 +0.88%)의 면역결핍치료제 ‘IVIG-SN 10%’와 메지온(187,000 +3.60%)의 ‘쥴비고’(성분명 유데나필)는 1분기 내에 FDA 승인 여부가 결정될 것으로 봤다. 제조시설 결함으로 지난 8월 최종보완요구서(CRL)를 수령한 한미약품(264,000 +0.38%)의 ‘롤론티스’는 품목허가(BLA) 재신청이 상반기 내 이뤄진다면 내년 중 FDA 승인이 가능할 것이란 전망이다.
유한양행(59,800 +1.70%)·오스코텍(29,900 +1.18%)의 ‘렉라자’(성분명 레이저티닙)는 올해 유럽종양학회(ESMO)에서 발표한 임상 결과를 근거로 가속 승인을 신청한다면, 내년 허가 및 출시가 가능할 것으로 예상했다. 레이저티닙은 2019년 얀센에 기술이전됐다.
최선호주로는 삼성바이오로직스(892,000 +6.06%)와 유한양행을 제시했다. 삼성바이오로직스에 대해서는 내년에도 위탁생산(CMO) 수요는 꾸준할 것이라며 빠른 증설을 통해 이에 대응할 수 있을 것이라 분석했다.
박 연구원은 “삼성바이오로직스는 4공장 증설에 이어 제2바이오캠퍼스에 들어설 5~6공장 증설도 계획 중”이라며 “5~6공장에는 기존의 동물세포 CMO 설비 외에 추가로 유전자·세포 치료제(GCT) 설비가 포함될 예정으로 이를 통해 기업의 장기적인 성장 그림이 확인돼 이에 따른 재평가(리레이팅)가 전망된다”고 했다.
유한양행에 대해서는 내년부터 R&D 투자의 결실을 맺을 것이라 봤다. 레이저티닙이 타그리소 내성 환자 대상 우수한 반응률을 보인 만큼 내년 가속 승인을 통한 글로벌 시장 진출을 기대했다.
이도희 기자
ⓒ 한경닷컴, 무단전재 및 재배포 금지
관련링크
댓글목록
등록된 댓글이 없습니다.

