[바이오번역 한경바이오트랜스] 녹십자 코로나19 혈장분획치료제, 임상 2상 승인
페이지 정보
작성자바이오트랜스 작성일 20-08-21 09:01본문
<한경바이오트랜스는 (주)한국경제신문이 운영하는 제약, 임상, 의학, 약학 분야에 특화된 바이오산업 전문 번역업체입니다.>
식품의약품안전처는 신종 코로나바이러스 감염증(코로나19) 혈장분획치료제 'GC5131'에 대해 임상 2상을 승인했다고 20일 밝혔다. 이로써 현재 국내에서 코로나19와 관련해 진행 중인 치료제 및 백신의 임상시험은 총 16건(치료제 14건, 백신 2건)이 됐다.
GC5131은 GC녹십자(283,500 -5.81%)에서 코로나19 완치자의 혈장을 이용해 개발 중인 고면역글로불린 성분의 의약품이다. 코로나19 환자를 대상으로 안전성과 유효성을 평가하는 임상 2상을 진행하게 된다.
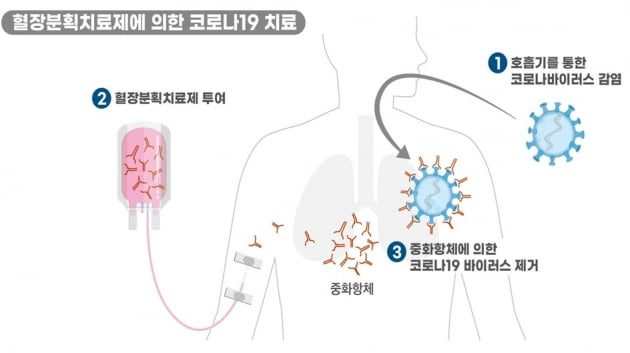
이 후보물질은 코로나19 완치자의 혈액 중 혈장을 대량으로 수집한 후 여러 공정을 거쳐 제품화한 것이다. 코로나19 바이러스를 무력화하는 중화항체가 농축된 면역글로불린이다. 면역글로불린이란 혈장 성분 중 면역에 중요한 역할(항원-항체반응)을 하는 단백질이다.
프랑스 중국 일본 이탈리아에서도 혈장분획치료제를 개발 중이다. 현재 6개의 소규모 임상시험이 진행 중에 있다.
코로나19 치료제를 개발하는 국내 기업은 부광약품(37,500 +5.34%)(임상 2상) 엔지켐생명과학(125,700 -4.05%)(임상 2상) 신풍제약(93,200 +11.62%)(임상 2상) 종근당(210,500 +7.95%)(임상 2상) 크리스탈(15,000 +5.26%)지노믹스(임상 2상) 대웅제약(115,000 +3.14%)(임상 2상) 셀트리온(305,000 +0.33%)(임상 1상) 제넥신(127,500 +0.55%)(임상 1b상) 녹십자(임상 2상) 등이 있다. 제넥신은 백신(임상 1·2a상)도 개발 중이다.
한민수 기자 hms@hankyung.com
ⓒ 한경닷컴, 무단전재 및 재배포 금지
관련링크
댓글목록
등록된 댓글이 없습니다.

